Порфирин Определение
Порфирин – большое кольцо молекула состоящий из 4 пирролов, которые представляют собой более мелкие кольца из 4 атомов углерода и 1 азота. Эти пиррольные молекулы связаны друг с другом через ряд одинарных и двойных связей, которые образуют молекулу в большое кольцо. Техническое название для 4 пирролов, соединенных вместе, – тетрапиррол. Кольцо плоское в пространстве, и распределение электронов практически одинаково по окружности кольца. По этой причине порфирин считается ароматическим соединением. Это означает, что молекула порфирина очень стабильна. Модель общего порфирина называется порфином. Эта молекула редко встречается в природе как промежуточное звено, но она является основой всех порфириновых молекул. Порфина можно увидеть ниже.
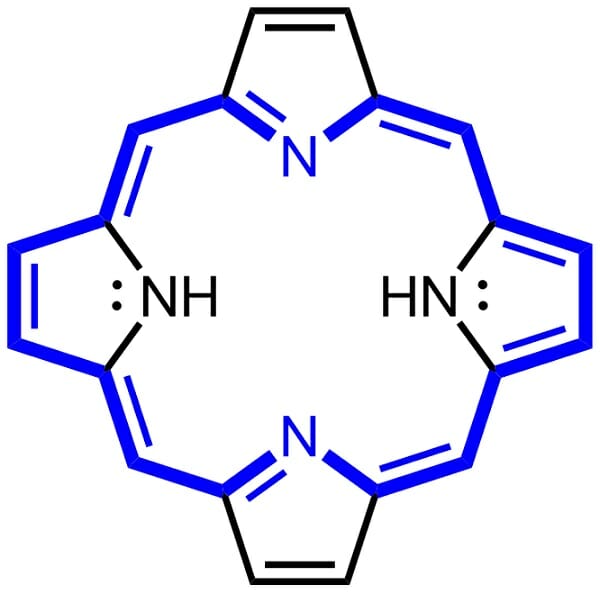
Синие части молекулы представляют собой ароматическое кольцо, которое составляет основу всех молекул порфирина. Черные молекулы и связи в конечном итоге заменят сложные боковые цепи. Эти молекулы позволят клеточному механизму прикрепиться и использовать порфирин. Порфирины также способны поглощать определенные длины волн света, особенно когда они связаны с различными ионами. Порфирины вызывают как красный цвет кровь и зеленый цвет растений, как обсуждается ниже.
Молекулы порфирина служат ряду целей у животных, растений и даже бактерии, По этой причине порфирин считается эволюционно консервативной молекулой. Это означает, что из-за его полезности бесчисленные линии организмов использовали и модифицировали порфирины, чтобы соответствовать их потребностям.
Типы порфиринов
Порфирины у животных
Основное использование молекул порфирина у животных заключается в создании гем групп. Эти молекулы являются просто молекулой порфирина с различными боковыми цепями, замещенными вокруг основного кольца. В гем, порфириновое кольцо выполняет важную функцию. Молекулы азота в центре кольца способны «содержать» молекулу железа. Именно эта порфириновая структура, содержащая железо, придает крови красный цвет. Хотя азот технически не связывается с молекулой железа, тем не менее он удерживается на месте под воздействием молекул азота и их распределения в пространстве. Общий гем можно увидеть ниже.
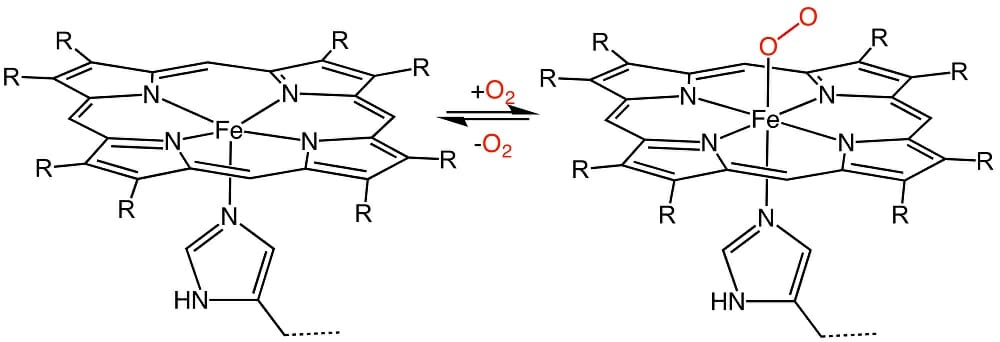
Основное назначение гема – транспортировка кислорода. Это можно увидеть на изображении выше. Когда кислород связан с гемом, он может быстро транспортироваться по всему организму и через клетки. Существует определенный белок, связанный с каждой частью тела, которая использует гемы для транспорта кислорода. Эритроциты содержат белок гемоглобин, который удерживает гем на месте. Эти белки также придают функциональность гему. Например, когда гемоглобин находится в кислой среде, он меняет форму. Это изменение формы заставляет кислород отделяться от гема. Этот механизм развился, потому что углекислый газ делает кровь кислой и является побочным продуктом использования кислорода. Поэтому, когда уровень углекислого газа высок, клеткам нужно больше кислорода. Этот механизм гемоглобина позволяет кислороду быть выпущенным в правильных частях тела.
Другая молекула, удерживающая гем, миоглобин, действует как молекула, транспортирующая кислород в мускул клетки. Этот гем также сделан из порфирина и содержит железо. Миоглобин имеет другие боковые цепи, чем гемоглобин. Как таковой, он может взаимодействовать с механизмом мышечных клеток и доставлять кислород с поверхности клетка к митохондрии которые нуждаются в кислороде окислительного фосфорилирования, Гемовые группы, состоящие из молекул порфирина, также обнаруживаются в молекулах цитохрома цепь переноса электронов, Здесь молекула железа действует как хранилище для дополнительных электронов. Он берет электроны, когда это необходимо, и освобождает их в другое время. Цепочка переноса электронов представляет собой сложную серию белков цитохрома, каждый из которых содержит гемовую группу. Они работают в унисон, чтобы передавать энергию электронам, приводя в действие протонный насос и накапливая энергию в форме АТФ.
Молекула порфирина – это органическая молекула, которая должна создаваться и разрушаться определенными белками в организме. Поскольку белки программируются ДНК, любые мутации в ДНК могут вызвать сбои в белке, которые обрабатывают молекулы порфирина. Хотя порфирин, как правило, чрезвычайно полезен, он не сформировался должным образом или не может быть разрушен, но представляет серьезную угрозу для организма. Молекулы порфирина очень интерактивны. Они могут нарушить клеточная мембрана и поскольку они содержат молекулу железа с потенциалом действовать в качестве поглотителя электронов, они способствуют образованию свободных радикалов.
Генетическое состояние, которое вызывает накопление порфиринов из-за невозможности их разрушения или правильного создания, называется порфирией. Существует много видов порфирий, в зависимости от которых фермент мутирует. Из-за этого существует множество симптомов и методов лечения для разных версий. В конечном счете, молекула порфирина, которая вызывает проблему, должна быть идентифицирована и решена. Это может означать замену искусственного порфирина или введение пациента через ген терапия, чтобы заставить их организм производить правильные ферменты. Порфирия часто диагностируется мочой пурпурного цвета, вызванной неразбитыми порфиринами, оставленными в моче.
Порфирины в растениях
Поскольку порфириновые молекулы эволюционно консервативны, мы видим те же железосодержащие гемопорфирины в растениях, что и у животных. Растения также используют цепь переноса электронов для производства АТФ, и такие же порфирины используются, как и у животных.
Однако растения также освоили другую конфигурацию молекулы порфирина, что позволяет им улавливать энергию при солнечном свете. хлорофилл это специальная молекула, созданная вокруг порфириновой основы. Как видно ниже, молекула хлорофилла имеет несколько уникальных боковых цепей от молекулы порфирина. У этого также есть действительно длинная боковая цепь, замеченная, сходя с основания. Эти боковые цепи слегка изменяют форму и конфигурацию базового порфирина.

Вы заметите, что вместо железа (Fe) в порфирине «захвачен» ион магния (Mg). В отличие от гемовых групп, которые содержат железо, магний в хлорофилле не способен переносить кислород. Вместо этого молекула функционирует для захвата энергии солнечного света. Ион магния помогает захватывать и хранить электроны во время процесса. Ион магния также помогает порфирину поглощать красный и синий свет, а не отражать красный свет, как это происходит с кровью. Это вызывает только сильный зеленый цвет, который дает растениям зеленый цвет.
Другие порфирины
Помимо растений и животных, порфирины есть практически повсюду в мире. Бактерии используют порфирины аналогично клеткам животных, хотя конечные молекулы, которые они используют, могут сильно отличаться от гемов у животных. Некоторые бактерии также обладают способностью к фотосинтезу, и, подобно растениям, они используют порфирины для захвата энергии солнца. Существуют также вещества, такие как витамин B12, которые синтезируются из порфирина, но едва ли похожи по составу.
Порфирины также могут быть синтезированы в лаборатории. Эти молекулы, потому что они действуют как пигменты, используются в красителях и в качестве цвета в различных растворах. Хотя мы можем синтезировать многие порфирины в лаборатории, они, как правило, более симметричны, чем природные порфирины. Это потому, что наш организм использует ферменты, разработанные тысячелетиями, для придания порфиринам полезной формы. Наше понимание биохимия еще не достаточно продвинут, чтобы повторить эти процессы в лаборатории.
Еще один интересный пример порфиринов можно найти в сырой нефти. По-видимому, в течение многих столетий, похороненных под Землей, органические молекулы могут естественным образом превращаться в порфирины. Эти вещества обнаруживаются в качестве побочных продуктов при добыче сырой нефти из земли. Ученые-эволюционисты выдвинули гипотезу, что эти порфирины и те, которые были созданы подобными методами, могли быть исходным материалом, с которого впервые возникла жизнь на Земле.
викторина
1. В настоящее время известно 9 видов порфирий. Какое из следующих утверждений точно описывает причину этого?A. Гены, кодирующие ферменты, изменяющие порфирин, могут мутировать во многих отношениях.B. Различные типы порфирий просто представляют разные симптомы для одной и той же болезниC. Все 9 типов вызваны одним и тем же геном
Ответ на вопрос № 1
верно. Существует много генов, кодирующих ферменты, которые работают с молекулой порфирина. Без них или с плохо функционирующими ферментами промежуточные продукты или продукты этих реакций начнут накапливаться. Этот избыток молекул порфирина вызывает повреждение тканей и наблюдаемых симптомов. Симптомы будут отличаться в зависимости от того, какой фермент в цепи нарушен.
2. Растения, животные и бактерии используют разновидность белка цитохрома, в котором содержится гем на основе порфирина. Что это говорит нам об эволюции?A. НичегоB. Эти организмы имеют общего предкаC. Эти организмы не имеют общих предков
Ответ на вопрос № 2
В верно. Генетический анализ генов, которые кодируют эти белки, показывает, что все они поразительно похожи друг на друга. Поскольку маловероятно, что каждая линия животных в отдельности выделяла этот белок, чтобы помочь использовать молекулы порфирина, следует предположить, что растения, животные и бактерии имеют общего предка.
3. Порфина, основная молекула порфирина, не встречается в природе. Почему это?A. Порфина можно создать только в лабораторииB. Порфин является промежуточным звеном; клетки сразу прикрепляют функциональные боковые цепиC. Порфин создан исключительно редкими организмами
Ответ на вопрос № 3
В верно. Порфина не видно в природе, потому что сам по себе он не функционирует. Чтобы быть функциональным порфирином, боковые цепи должны влиять на электрическую активность кольца. Это заставило кольцо схватиться за ион и нести его вокруг. Различные ионы, переносимые порфириновыми кольцами, определяются боковыми цепями, влияющими на их электрическую активность.
Ссылки
- Lodish, H., Berk, A., Kaiser, C.A., Krieger, M., Scott, M.P., Bretscher, A.,. , , Мацудайра, П. (2008). Молекулярно-клеточная биология (6-е изд.). Нью-Йорк: W.H. Фримен и Компания.
- McMahon, M.J., Kofranek, A.M. & Rubatzky, V.E. (2011). Растение Наука: рост, развитие и использование культурных растений (5-е изд.). Бостон: Прентинс Холл.
- Нельсон Д.Л. и Кокс М.М. (2008). Основы биохимии. Нью-Йорк: W.H. Фримен и Компания.